Лекція 2: Єдність хімічного складу живих організмів.
План.
1. Вивчення елементарного складу живих організмів.
2. Неорганічні сполуки: вода і мінеральні солі.
Терміни та поняття: макроелементи, мікроелементи, органогенні та біогенні елементи, гемоціанін. Атоми живого і періодична система хімічних елементів.
Як відомо з курсу хімії, до складу тіл живої й неживої природи входять хімічні елементи. Живі організми утворені з тих самих атомів, що й тіла неживої природи. Встановлено, що в клітинах у різній кількості міститься близько 80 природних елементів періодичної системи Д.І. Менделєєва. (Пригадайте загальну кількість хімічних елементів, відомих науці.) Тому відмінність у елементному складі живого й неживого полягає лише в різному кількісному співвідношенні хімічних елементів, а не в тому, що у клітинах організмів містяться атоми особливих хімічних елементів, яких більше ніде немає. Наприклад, Силіцій (Sі) — другий за масою елемент земної кори (пригадайте, пісок — це ніщо інше, як силіцій(IV) оксид SiO2) — у клітинах живих організмів становить менше 0,0001 % і не входить навіть до двадцяти найпоширеніших елементів живого. Проте в живій речовині накопичуються елементи з певними властивостями. Так, відмічено, що найбільше живої маси складають елементи Карбон, Нітроген, Фосфор, Сульфур (C, N, P, S), що легко утворюють розчинні та газуваті сполуки, хоча в земній корі їх вміст відносно незначний. Навпаки елементи, що зазвичай утворюють нерозчинні у воді сполуки — Сіліцій, Ферум, Алюміній (Si, Fe, Al), у складі організмів зустрічаються в мізерній кількості, хоча є головними в неживій природі. Взагалі між біологічною роллю елемента та його положенням у періодичній системі є певна відповідність. Перш за все, органічний світ побудований з легких атомів. Крім того, при переході від легких до важких елементів у межах однієї підгрупи підвищується токсичність.
Основні органогенні елементи – на їх частку припадає майже 98 % хімічного вмісту клітини – кисень, вуглець, водень та нітроген.
Макроелементи – фосфор, калій, кальцій, сірка, хлор, магній, натрій, залізо – сумарна частка 1,9 %.
Мікроелементи – йод, кобальт, марганець, мідь, молібден, цинк, тощо до 50 видів.
Ультрамікроелементи – свинець, бром, срібло, золото.
Кисень (65 % від маси клітини) – входить до складу води та біомолекул, приймає активну участь в утворенні енергії в клітинах у вигляді
АТФ – аденозинтрифосфорної кислоти.
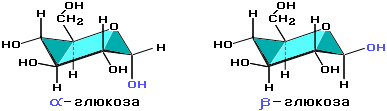
Вуглець (15 – 18 % від маси клітини) – входить до складу біомолекул, вуглевод глюкоза є основним джерелом енергії, яка утворюється під час гліколізу та кисневого розщеплення глюкози.
Водень – (8 - 10 % від маси клітини) входить до складу води та біомолекул.
Нітроген – (1,5 – 3,0 %) структурний компонент білків, нуклеїнових кислот, АТФ і деяких інших біомолекул.
Фосфор – (0,2 – 1 %) входить до складу кісток, білків, мембран клітин у складі фосфоліпідів.
Калій – (0,15-0,4 %) основний позитивно заряджений іон в організмі тварин.
Сірка – (0,15 – 0,2 %) – входить до складу білків та інших біомолекул.
Хлор – (0,05 – 0,1 %) – негативно заряджений іон в організмі тварин.
Кальцій – (0,04 – 0,2 %) – основний компонент кісток, іони кальцію регулюють скорочення м’язів людини та ссавців.
Магній – (0,02 – 0,03 %) – активує діяльність ферментів, структурний компонент хлорофілу.
Натрій – (0,02 – 0,03 %) – головний внутрішньоклітинний позитивно заряджений іон.
Залізо - (0,01 – 0,15 %) – входить до складу багатьох біомолекул, в тому чслі гемоглобіну.
Мікроелементи, що входять до складу організму людини.
Далі інформація буде скомпонована за таким принципом:
Назва мікроелемента Хім. символ Доля у заг. масі Роль та функції елемента в організмі.
Мікроелементи:
Йод I Сліди . Регуляція роботи щитоподібної залози.
Кобальт Co Сліди Входить до складу біоактивного комплексу вітаміну В 12 (цианокобаламіну)
ВОДА:
Електронейтральна але полярна. Водневий зв’язок виникає між атомами водню і кисню за рахунок утворення спільної пари електронів по одному від кожного атома. Вода визначає внутрішньоклітинний тиск. Вода формує водяну оболонку навколо білків що перешкоджає їх взаємодії – така вода називається зв’язаною (структурованою). Розчинні у воді сполуки – гідрофільні і полярні. Погано розчинні у воді сполуки – гідрофобні та неполярні. До гідрофільних сполук належать кристалічні солі, наприклад кухонна сіль. До гідрофобних сполук відносять всі ліпіди, деякі білки, які містять неполярні групи ( - СН2, - СН2, СН3). Важливу роль грає водневий показник рН. Контроль стану водойм – джерел водопостачання, свердловин та інших джерел води та підтримка їх в належному стані є життєважливим завданням сучасного світу.

Загальні вимоги до питної води:
1. Вода повинна бути безпечною в епідеміологічному і радіаційному відношенні
2. бути безпечною за хім. складом
3. мати прийнятні органолептичні властивості.
У Україні ці вимоги регламентовані санітарним законодавчим документом ДСАНПіН (Державниі санітарні правила і норми «Вода питна». Гігієнічні вимоги до якості води централізованого господарсько-питного водопостачання № в 383 від 23. 12. 1996 р.)
Для оцінки якості питної води проводять наступні заходи:
Визначення загального мікробного числа води:
Мікробне число води це – кількість мікробів в 1 мл води.
Визначення колі-індексу:
Колі-тітр води – це мінімальне кол. води, в якій виявляють бактерії групи кишкових паличок
Колі-індекс води – це кількість кишкової палички. у 1 л води
Органолептичний аналіз води:
Визначення показників безпеки хімічного складу питної води.
Визначення соди. хлоридів
Визначення залишкового хлору в питній воді
Молекула води ( H2O) складається з 2 двох атомів водню (H) і одного атома кисню (O). Відповідно до електронної будови атомів водню і кисню молекула води має в своєму розпорядженні п'ять електронних пар. Вони утворюють електронну хмару. Хмара неоднорідна – в ній можна розрізнити окремі згущення і розрідження. У кисневого ядра створюється надлишок електронної щільності. Внутрішня електронна пара кисню рівномірно обрамляє ядро.
У періодичній системі елементів Д.І. Менделєєва кисень утворює окрему підгрупу. Вона так і називається: підгрупа кисню. Елементи, що входять в неї: кисень, сірка, селен і телур мають багато загального у фізичних і хімічних властивостях. Спільність властивостей просліджується, як правило, і для однотипових з'єднань, утворених членами підгрупи. Проте для води характерний відхилення від правил. З найлегших з'єднань підгрупи кисню (а ними є гідриди) вода – найлегша. Фізичні характеристики гідридів, як і інших типів хімічних сполук, визначається положенням в таблиці елементів відповідної підгрупи. Так, чим легший елемент підгрупи, тим вище летючість його гідриду. Тому в підгрупі кисню найвищої повинна бути летючість води–гідриду кисню. Ця ж властивість виявляється і в здатності води «прилипати» до багатьох предметів, тобто змочувати їх.
Температура кипіння води +100°С, замерзання – 0°C. Це наочна перевага асоціативності – широкий температурний інтервал існування, можливість здійснити всі фазове стани в умовах нашої планети. Асоціативність води позначається і на дуже високій питомій теплоті її паротворення. Щоб випарувати воду, вже нагріту до 100°С, потрібно в шестеро більше кількості теплоти, чим для нагріву цієї ж маси води на 80°С (від 20 до 100°С).
Питома теплота плавлення льоду більш висока, чим у багатьох речовин, вона еквівалентна витраті кількості теплоти під час нагрівання 1 г води на 80°С (від 20 до 100°С).
Здатність води накопичувати великі запаси теплової енергії дозволяє згладжувати різкі температурне коливання на земній поверхні в різні пори року і у різний час доби. Завдяки цьому вода є основним регулятором теплового режиму нашої планети. У людини при загальному змісті води 60% маси тіла, внутріклітинна вода складає 40%, міжклітинна рідина - 16%, внутрішньосудинна - 4,5%.
Характер фізико-хімічних процесів в тканинах визначають іони (Na+, К+, Са+ Mg2+, C1-, SO4 , HCO3- і ін.), а також мікроелементи. Всмоктування електролітів в кишечнику, забезпечує надходження солей в кров. З кров'ю або лімфою вони переносяться до клітин організму. По сольовому складу поза- і внутрішньоклітинні рідини різко розрізняються: у клітинах високий зміст К+ Mg2+ і фосфатів, поза клітинами - Na+, Ca2+, Cl-. Іонна асиметрія забезпечується діяльністю плазматичних мембран і скріпленням ряду іонів хімічними компонентами клітин. Усередині клітин іони також розподілені нерівномірно: Na+ більше в ядрі, чим у цитоплазмі, Са2+- в мітохондріях. Характер водного обміну визначається типом осморегуляції, яка робить вплив і на стан систем виділення солей. У ссавців основним органом регуляції балансу води і солей являються нирки. Регуляція В.-с. о. здійснюється спец. рефлекторними системами, одна з яких реагує на зміну об'єму рідин (волюморегуляція), інша - їх осмотичні концентрації (осморегуляція); виявлені специфічні системи регуляції балансу окремих іонів. Зменшення об'єму крові рефлекторно стимулює секрецію вазопресину і альдостерону, який утримує Na+ у організмі. Надлишок Ca2+ у крові підвищує секрецію кальцитоніну, що знижує його концентрацію в крові за рахунок переходу в кістки і виділення нирками; гіпокальціємія сприяє секреції паратиреоїдного гормону, що підсилює резорбцію Ca2+ з кістки і що зменшує його виділення нирками. Діяльність органів і систем, що забезпечують водно-сольовий гомеостаз, координується ЦНС. В процесі еволюції зростає точність і ефективність механізму регуляції. Кров (sanguis), циркулююча в кровоносній системі всіх хребетних і деяких безхребетних тварин - «рідка тканина внутрішнього середовища, являється тканиною, забезпечує життєдіяльність ін. тканин і клітин, а також виконання ними різних. функцій в цілісному організмі. Основні функції К.: дихальна - транспортує гази (О2 - від органів дихання до тканин і СО2 - від тканин до органів дихання); трофічна і екскреторна - переносить поживні речовини (глюкозу, амінокислоти, солі і т. п.) від органів травлення до тканин, а кінцеві продукти обміну (сечовина, креатин і ін.) - до органів виділення; регуляторна - бере участь в гуморальній регуляції (переносить гормони і ін. біологічно активні речовини), підтримує водно-сольовий обмін і кислотно-лужну рівновагу, грає важливу роль в підтримці постійної температури тіла; захисна - містить антитіла, антитоксини, лізіни, а також лейкоцити, здатні руйнувати і поглинати чужорідні агенти. Плазма містить проміжні і кінцеві продукти обміну речовин, солі, гормони, вітаміни, ферменти. Істотну частину крові складають білки - дихальні пігменти, білки строми еритроцитів і ін. формених елементів, а також білки плазми - альбуміни, глобуліни і фібріноген (плазма без фібріногену - сироватка крові). Вуглеводи представлені головним чином глюкозою. Складна суміш ліпідів крові включає нейтральні жири, вільні жирні кислоти і продукти їх розпаду, холестерин, стероїдні гормони і ін. У людини об'єм крові у нормі складає в середньому у чоловіків 5,2 л, у жінок 3,9 л, при цьому її частина, іноді до 50%, може знаходитися в т.з. депо крові (селезінка, печінка).
Серед незвичайних властивостей води важко обійти увагою ще одне – її виключно високе поверхневе натягнення 0,073 Н/м (при 20°С). Зі всіх рідин болем високе поверхневе натягнення має тільки ртуть. Воно виявляється в тому, що вода постійно прагне стягнути, скоротити свою поверхню, хоча вона завжди приймає форму ємкості, в якій знаходиться в даний момент. Вода лише здається безформною, розтікаючись по будь-якій поверхні. Сила поверхневого натягнення примушує молекули її зовнішнього шару зчіплюватися, створюючи пружну зовнішню плівку. Властивості плівки також визначаються замкнутими і розімкненими водневими зв'язками, асоціатами різної структури і різного ступеня впорядкованості. Завдяки плівці деякі предмети, будучи важчі за воду, не занурюються у воду (наприклад, обережно покладена на воду сталева голка).
Сольовий склад річкових і морських вод різний не тільки кількісно, але і якісно. На 89% морські солі складаються з хлоридів (переважно – натрію і кальцію), на 10%–з сульфатів (натрію, калія і магнію), на 1% – з карбонатів (натрію і кальцію), а також незначних кількостей інших солей. У прісних водах набір мінеральних домішок виглядає інакше. Більше всього тут карбонатів (натрію і кальцію) –до 80%. Сульфатів (натрію, кальцію і магнію)– біля 13%. 7% приходяться на хлориди (натрію і кальцію) і інші солі. З газів в прісних і морських водах найширше представлені кисень, азот, вуглекислий газ, сірководень. У чистих холодних стоках гірських річок зміст кисню може досягати 6 мг/л. У глибинних шарах Чорного моря висока концентрація сірководню – до 100 мг/л. Цей отруйний газ присутній і в нижніх шарах деяких озер. У прісних і морських водах в невеликих кількостях є і різноманітні органічні компоненти – розчинні з'єднання типу білків, цукрів, спиртів, вуглеводів. Це продукти життєдіяльності і розпаду тваринних і рослинних організмів, що населяють водоймища і їх береги, а також відходи промисловості і сільського господарства.
Капілярність води При вивченні цього явища встановили, що всі речовини, які легко змочуються водою (глина, пісок, скло, папір і ін.), неодмінно мають в своєму складі атоми кисню. Для пояснення природи змочування цей факт виявився ключовим: енергетично неврівноважені молекули поверхневого шару води дістають можливість утворювати додаткові водневі святи з «сторонніми» атомами кисню. Завдяки поверхневому натягненню і здібності до змочування, вода може підніматися у вузьких вертикальних каналах на висоту більшу ніж та, яка допускається силою тяжіння, тобто вода володіє властивістю капілярності. Капілярність грає важливу роль в багатьох природних процесах, що відбуваються на Землі. Завдяки цьому вода змочує товщу ґрунту, лежачу значно вище за дзеркало ґрунтових вод і доставляє корінню рослин розчини живильних речовин. Капілярністю обумовлено рух крові і тканинних рідин в живих організмах.
Епідеміологічне значення води.
Основу мікробної клітини складає вода - 80 - 90 % загальної маси. Вода є переносником мікроорганізмів як сапрофітних так і хвороботворних.
Escherichia coli серотип O157:H7 - основна причина розладів травлення. Інфекція викликана цією бактерією часто приводить до кривавого проносу, і іноді до ниркового недоліку. Люди можуть заразитися з E.coli O157:H7 багатообразними шляхами. Заразитися можна п'ючи заражену для стічних вод воду.
Холера - гостра інфекційна хвороба, викликана інфекцією кишечнику бактерійним вібріоном cholerae.
Люди стають зараженими Leptospira через контакт з водою, продовольством, або сечею, що містить лептоспір, від цих заражених тварин. Це, можливо, трапляється під час ковтання зараженого продовольства або води або через контакт шкіри, особливо з поверхнями, які відносяться до слизової оболонки, як наприклад очі або ніс, або з розбитою шкірою
Солі.
неорганічних речовин перебувають в організмі або в іонному стані, або у вигляді твердих сполук. Катіони – калію, кальцію, натрію, магнію, тощо. Аніони – соляної , сірчаної, фосфорної, вугільної, тощо.
В сучасному світі важливу роль відіграють заходи щодо зниження рівня забруднення довкілля деякими хімічними елементами, неорганічними і органічними сполуками.
Мільярди років тому в холодній газопиловій хмарі, що з часом згустилася, ущільнилася і стала Землею, вже містилася вода. Швидше за все, вона була у вигляді крижаного пилу. Це підтверджують дослідження Всесвіту. Уставлено, що початкові елементи для утворення води — водень і кисень в нашій Галактиці належать до найпоширеніших речовин космосу.
Фізіологічне значення води
Добова потреба в воді – 1,5 і більше літрів на людину. З віком кількість води знижується. При порушенні водного балансу відбувається ряд порушень.
Гігієнічне значення води.
Добова потреба води залежить від регіону може досягати до 1000 літрів на людину. За відсутності центрального водопостачання 60 л.
Класифікація забруднення води:
1. Хвороботворними організмами.
2. Хімічне забруднення води
А. Неорганічними;
Б. Органічними;
В. Токсичними;
Г. Поверхнево-активними сполуками;
Епідеміологічне значення води. Близько напівмільярда людей хворіє на захворювання, які передаються через воду, 3 мільйони гине.
1. Бактерійні антропонози (дизентерія, холера)
2. Вірусні (гепатит, поліомієліт)
3. Зоонозні інфекції (лептоспіроз).
4. Паразитарні захворювання - захворювання лямбліоз), гельмінтози (геогельмінти)
5. Ендемічні захворювання. Пов'язані з мінеральним складом води.
Умови для розповсюдження хвороб: збудник повинен потрапити у воду, патогенні мікроорганізми повинні зберігати активність у воді, збудник повинен потрапити в організм.
Епідеміологічна характеристика спалахів захворювань.
1. Масовість (дифузна) При залповому забрудненні мікроорганізм може потрапити у водопровідну мережу і викликати захворювання.
2. Сезонність (рання весна)
3. За етіологічністю.
4. За клінікою: поліморфізм (різна по ступеню тяжкості клінічна картина)
5. Зниження ступеня тяжкості захворювань в динаміці.
6. Різкий підйом і повільний спад.
При харчовому: спалахи хвороби, різкий підйом і спад, приблизно однакові клінічні прояви.
Хімічний склад води.
1. Хімічні речовини присутні в будь-якому випадку.
2. Хімічні речовини, що потрапляють у воду в результаті дії людини.
Мінеральний склад води. У воді загальна мінералізація – хлориди сульфати. Впливають на органолептичні властивості.
Загальна мінералізація - солі хлору і сірки. Не вище 1 г на літр. Для питної води не більше 1г на літр. Якщо більше грама - мінеральна вода. Питна вода повинна бути без смаку. Мінеральна вода - з присмаком. Нормальна питна вода - 200-400 мг на літр. Вода з показниками вище - є слабкомінералізованою.
Жорсткість води. Постійна і усунена жорсткість. Усунена - при кип'яченні випадають в осад.
При зміні жорсткості води можуть спостерігатися диспепсичні розлади. До 7 міліграм на літр.
Азотисті сполуки. Визначаються в будь-якій воді. Утворюються при окисненні органічних речовин у воді. При кип'ятінні знищуються сапрофітні бактерії, що з часом приводить до погіршення органолептичних властивостей води.
Коло обіг нітрогену в воді:
Аміак—нітрити—нітрати.
По концентрації цих сполук можна говорити про органічне забрудення води.
Метгемоглобінемію викликають нітрити.
Ендемічні захворювання.
Флюороз. Проявляється зміною суглобів. Остеопороз, тугорухливість суглобів.
Ендемічний зоб. Нестача в воді йоду, або наявність великої концентрації сполук, які його зв’язують
Хімічні речовини, що ПОТРАПЛЯЮТЬ У ВОДУ, ЧАСТО МАЮТЬ АНТРОПОГЕННУ ДІЮ.
В РОЗЧИНЕНОМУ СТАНІ БІЛЬШЕ 3000 ХІМІЧНИХ СПОЛУК у водоймищах.
ГДК - гранично допустима концентрації.
1. Вивчення вплив речовини на органолептичні властивості води.
2. Вивчення токсичних властивостей речовини.
3. Вплив речовини на процеси самоочищення водоймищ.
Визначається лімітуючий показник, на підставі якого встановлюється ГДК.
Якість води – вивчення:
1 етап - органолептичні властивості.
2 етап - почало 19 століття. У Брюсселі документ, що НОРМУЄ хімічний склад води
3 етап - мікробіологічні показники.
4 етап - всі разом з середини минулого століття.
Вимоги до питної води.
1. Повинна відповідати безпеці, нешкідлива і сприятлива.
2. Якість води повинне відповідати нормі не тільки на водопровідній станції, але і в місцях використання.
3. Безпека питної води визначається по нормативу, що характеризує мікробну, вірусну і паразитарну дію.
4. Нешкідливість визначається по 3 групам показників
А. Узагальнені показники хімічних речовин, які містяться в природних умовах.
Б. Ті що утворюються у воді при очищенні або знезараженні.
В. Токсичні хімічні речовини.
5. Мікробіологічні показники.
Органічне забруднення води
Визначається по азотистих з'єднаннях.
Окислюваність води - та кількість кисню, яка необхідна для окислення органіки.
Біохімічна потреба кисню - та кількість кисню, яка необхідна для біохімічного окислення води.
Мікробіологічні показники.
Паразитарне забруднення
Водневий показник Нормативи 6-9 рН
Гігієнічні вимоги щодо якості питної води та її санітарна оцінка на Україні. В Україні ці вимоги регламентовані санітарним законодавством - документом ДСАНПіН (Державні санітарні правила і норми «Вода питна». Гігієнічні вимоги до якості води централізованого господарсько-питного водопостачання № 383 від 23. 12. 1996 р.)
Мікробіологічну чистоту води визначають за такими параметрами:
Мікробне число води це – кількість мікробів в 1 мл води.
Визначення колі-індексу.
Визначення колі титру.
Визначення вмісту хлору у воді;
Визначення залишкового хлору у питній воді.
ПДК за мікроорганізмами води для пиття.
Колі-титр води – мінімальна кількість води, в якій виявляють бактерії групи кишкової палички – норми визначення не менше 300
Колі-індекс води– це кількість кишкової палички в 1 л води – норми визначення не більше 3.
Жодної цисти лямблій в 50 літрах води.
Централізоване водопостачання.
Гігієнічна характеристика джерел водопостачання.
Вимоги: доступність вододжерела, достатня водоємність джерела. Повинна бути в 1000 разів більше, НІЖ необхідно для населеного пункту, інтенсивність забруднення повинна піддаватися усуненню.
Джерела води: підземні, поверхневі.
Розташування джерел води.
Проточні і непроточні. Вода відкритих вододжерел коливається за складом залежно від пори року. Найбільш стабільними в цьому показники є оліготрофні озера. На глибині 10м забруднення і склад постійні.
Підземні води найбільш якісні. Діляться на ґрунтові і міжпластові. Глибина залягання - 2-4 метри.
Найбільш хороша - міжпластова.
Свердловини бувають напірні або артезіанські і безнапірні.
Якість води зі свердловин оптимальна. Хімічний склад залежить від геологічного складу ґрунту.
Методи очищення:
Барабанні мікро фільтри - від грубої суспензії. Розмір часток 0.1мм. Близько 40% частинок затримуються. Майже 100% розчинених сполук не затримуються.
Коагуляція Процес укрупнення колоїдних домішок за рахунок їх взаємного злипання. Солі алюмінію, заліза. До 80% хімічних речовин адсорбуються. Додають флоккулянти - сполуки, прискорюючі коагуляцію.
Відстоювання води.
У відстійниках флокційні методи є додатковими при відстоюванні. Особливості - для видалення поверхнево-активних речовин.
Фільтрація води - Піщані фільтри. 1-1.5 м. Повільна і швидка фільтрація. Найбільш небезпечна з погляду хімічної сполуки. Насипні, іонообмінні фільтри, полупроникні мембрани. Адсорбційні фільтри. Активоване вугілля, де структура фільтру нагадує сир.
Знезараження води. Може бути хімічним і фізичним.
При використанні фізичних методів неможливо швидко визначити якість води. 90% води в світі хлорується. Використовується газоподібний хлор частіше за все при централізованому водопостачанні в крупних містах. Активну дію забеспечує або хлор, або хлоорноватиста кислота.
Гідробіологія, це наука про екологію води – наука, що вивчає взаємини людини, тварин. рослин. інших живих організмів з водневим навколишнім середовищем. Людина безпосередньо залежить від екологічної рівноваги, яка зберігає стабільність умов навколишнього середовища, без якого людина не мала б шансів вижити. А як відомо – основою життя на Землі є вода. У природі існує відносна стійкість видового складу живих організмів, їх чисельності, продуктивності, розподілу в просторі, а також сезонних змін, біотичний. колообіг речовин в будь-яких природних співтовариствах. Існує колообіг і води. Людина випиває і з’їдає за своє життя більше 50 тон води, білків біля 2,5 тон, жирів біля 2,0 тон, вуглеводів – 10 тон, солі – 30 кг. Накопичення майже незначної кількості шкідливих речовин в продуктах харчування може протягом часу призводити до значних змін з боку органів і систем і в решті решт негативно впливати на стан здоров’я людини .
План.
1. Вивчення елементарного складу живих організмів.
2. Неорганічні сполуки: вода і мінеральні солі.
Терміни та поняття: макроелементи, мікроелементи, органогенні та біогенні елементи, гемоціанін. Атоми живого і періодична система хімічних елементів.
Як відомо з курсу хімії, до складу тіл живої й неживої природи входять хімічні елементи. Живі організми утворені з тих самих атомів, що й тіла неживої природи. Встановлено, що в клітинах у різній кількості міститься близько 80 природних елементів періодичної системи Д.І. Менделєєва. (Пригадайте загальну кількість хімічних елементів, відомих науці.) Тому відмінність у елементному складі живого й неживого полягає лише в різному кількісному співвідношенні хімічних елементів, а не в тому, що у клітинах організмів містяться атоми особливих хімічних елементів, яких більше ніде немає. Наприклад, Силіцій (Sі) — другий за масою елемент земної кори (пригадайте, пісок — це ніщо інше, як силіцій(IV) оксид SiO2) — у клітинах живих організмів становить менше 0,0001 % і не входить навіть до двадцяти найпоширеніших елементів живого. Проте в живій речовині накопичуються елементи з певними властивостями. Так, відмічено, що найбільше живої маси складають елементи Карбон, Нітроген, Фосфор, Сульфур (C, N, P, S), що легко утворюють розчинні та газуваті сполуки, хоча в земній корі їх вміст відносно незначний. Навпаки елементи, що зазвичай утворюють нерозчинні у воді сполуки — Сіліцій, Ферум, Алюміній (Si, Fe, Al), у складі організмів зустрічаються в мізерній кількості, хоча є головними в неживій природі. Взагалі між біологічною роллю елемента та його положенням у періодичній системі є певна відповідність. Перш за все, органічний світ побудований з легких атомів. Крім того, при переході від легких до важких елементів у межах однієї підгрупи підвищується токсичність.
Основні органогенні елементи – на їх частку припадає майже 98 % хімічного вмісту клітини – кисень, вуглець, водень та нітроген.
Макроелементи – фосфор, калій, кальцій, сірка, хлор, магній, натрій, залізо – сумарна частка 1,9 %.
Мікроелементи – йод, кобальт, марганець, мідь, молібден, цинк, тощо до 50 видів.
Ультрамікроелементи – свинець, бром, срібло, золото.
Кисень (65 % від маси клітини) – входить до складу води та біомолекул, приймає активну участь в утворенні енергії в клітинах у вигляді
АТФ – аденозинтрифосфорної кислоти.
Вуглець (15 – 18 % від маси клітини) – входить до складу біомолекул, вуглевод глюкоза є основним джерелом енергії, яка утворюється під час гліколізу та кисневого розщеплення глюкози.

Нітроген – (1,5 – 3,0 %) структурний компонент білків, нуклеїнових кислот, АТФ і деяких інших біомолекул.
Фосфор – (0,2 – 1 %) входить до складу кісток, білків, мембран клітин у складі фосфоліпідів.
Калій – (0,15-0,4 %) основний позитивно заряджений іон в організмі тварин.
Сірка – (0,15 – 0,2 %) – входить до складу білків та інших біомолекул.
Хлор – (0,05 – 0,1 %) – негативно заряджений іон в організмі тварин.
Кальцій – (0,04 – 0,2 %) – основний компонент кісток, іони кальцію регулюють скорочення м’язів людини та ссавців.
Магній – (0,02 – 0,03 %) – активує діяльність ферментів, структурний компонент хлорофілу.
Натрій – (0,02 – 0,03 %) – головний внутрішньоклітинний позитивно заряджений іон.
Залізо - (0,01 – 0,15 %) – входить до складу багатьох біомолекул, в тому чслі гемоглобіну.
Мікроелементи, що входять до складу організму людини.
Далі інформація буде скомпонована за таким принципом:
Назва мікроелемента Хім. символ Доля у заг. масі Роль та функції елемента в організмі.
Мікроелементи:
Йод I Сліди . Регуляція роботи щитоподібної залози.
Кобальт Co Сліди Входить до складу біоактивного комплексу вітаміну В 12 (цианокобаламіну)
ВОДА:
Електронейтральна але полярна. Водневий зв’язок виникає між атомами водню і кисню за рахунок утворення спільної пари електронів по одному від кожного атома. Вода визначає внутрішньоклітинний тиск. Вода формує водяну оболонку навколо білків що перешкоджає їх взаємодії – така вода називається зв’язаною (структурованою). Розчинні у воді сполуки – гідрофільні і полярні. Погано розчинні у воді сполуки – гідрофобні та неполярні. До гідрофільних сполук належать кристалічні солі, наприклад кухонна сіль. До гідрофобних сполук відносять всі ліпіди, деякі білки, які містять неполярні групи ( - СН2, - СН2, СН3). Важливу роль грає водневий показник рН. Контроль стану водойм – джерел водопостачання, свердловин та інших джерел води та підтримка їх в належному стані є життєважливим завданням сучасного світу.

1. Вода повинна бути безпечною в епідеміологічному і радіаційному відношенні
2. бути безпечною за хім. складом
3. мати прийнятні органолептичні властивості.
У Україні ці вимоги регламентовані санітарним законодавчим документом ДСАНПіН (Державниі санітарні правила і норми «Вода питна». Гігієнічні вимоги до якості води централізованого господарсько-питного водопостачання № в 383 від 23. 12. 1996 р.)
Для оцінки якості питної води проводять наступні заходи:
Визначення загального мікробного числа води:
Мікробне число води це – кількість мікробів в 1 мл води.
Визначення колі-індексу:
Колі-тітр води – це мінімальне кол. води, в якій виявляють бактерії групи кишкових паличок
Колі-індекс води – це кількість кишкової палички. у 1 л води
Органолептичний аналіз води:
Визначення показників безпеки хімічного складу питної води.
Визначення соди. хлоридів
Визначення залишкового хлору в питній воді
Молекула води ( H2O) складається з 2 двох атомів водню (H) і одного атома кисню (O). Відповідно до електронної будови атомів водню і кисню молекула води має в своєму розпорядженні п'ять електронних пар. Вони утворюють електронну хмару. Хмара неоднорідна – в ній можна розрізнити окремі згущення і розрідження. У кисневого ядра створюється надлишок електронної щільності. Внутрішня електронна пара кисню рівномірно обрамляє ядро.
У періодичній системі елементів Д.І. Менделєєва кисень утворює окрему підгрупу. Вона так і називається: підгрупа кисню. Елементи, що входять в неї: кисень, сірка, селен і телур мають багато загального у фізичних і хімічних властивостях. Спільність властивостей просліджується, як правило, і для однотипових з'єднань, утворених членами підгрупи. Проте для води характерний відхилення від правил. З найлегших з'єднань підгрупи кисню (а ними є гідриди) вода – найлегша. Фізичні характеристики гідридів, як і інших типів хімічних сполук, визначається положенням в таблиці елементів відповідної підгрупи. Так, чим легший елемент підгрупи, тим вище летючість його гідриду. Тому в підгрупі кисню найвищої повинна бути летючість води–гідриду кисню. Ця ж властивість виявляється і в здатності води «прилипати» до багатьох предметів, тобто змочувати їх.
Температура кипіння води +100°С, замерзання – 0°C. Це наочна перевага асоціативності – широкий температурний інтервал існування, можливість здійснити всі фазове стани в умовах нашої планети. Асоціативність води позначається і на дуже високій питомій теплоті її паротворення. Щоб випарувати воду, вже нагріту до 100°С, потрібно в шестеро більше кількості теплоти, чим для нагріву цієї ж маси води на 80°С (від 20 до 100°С).
Питома теплота плавлення льоду більш висока, чим у багатьох речовин, вона еквівалентна витраті кількості теплоти під час нагрівання 1 г води на 80°С (від 20 до 100°С).
Здатність води накопичувати великі запаси теплової енергії дозволяє згладжувати різкі температурне коливання на земній поверхні в різні пори року і у різний час доби. Завдяки цьому вода є основним регулятором теплового режиму нашої планети. У людини при загальному змісті води 60% маси тіла, внутріклітинна вода складає 40%, міжклітинна рідина - 16%, внутрішньосудинна - 4,5%.
Характер фізико-хімічних процесів в тканинах визначають іони (Na+, К+, Са+ Mg2+, C1-, SO4 , HCO3- і ін.), а також мікроелементи. Всмоктування електролітів в кишечнику, забезпечує надходження солей в кров. З кров'ю або лімфою вони переносяться до клітин організму. По сольовому складу поза- і внутрішньоклітинні рідини різко розрізняються: у клітинах високий зміст К+ Mg2+ і фосфатів, поза клітинами - Na+, Ca2+, Cl-. Іонна асиметрія забезпечується діяльністю плазматичних мембран і скріпленням ряду іонів хімічними компонентами клітин. Усередині клітин іони також розподілені нерівномірно: Na+ більше в ядрі, чим у цитоплазмі, Са2+- в мітохондріях. Характер водного обміну визначається типом осморегуляції, яка робить вплив і на стан систем виділення солей. У ссавців основним органом регуляції балансу води і солей являються нирки. Регуляція В.-с. о. здійснюється спец. рефлекторними системами, одна з яких реагує на зміну об'єму рідин (волюморегуляція), інша - їх осмотичні концентрації (осморегуляція); виявлені специфічні системи регуляції балансу окремих іонів. Зменшення об'єму крові рефлекторно стимулює секрецію вазопресину і альдостерону, який утримує Na+ у організмі. Надлишок Ca2+ у крові підвищує секрецію кальцитоніну, що знижує його концентрацію в крові за рахунок переходу в кістки і виділення нирками; гіпокальціємія сприяє секреції паратиреоїдного гормону, що підсилює резорбцію Ca2+ з кістки і що зменшує його виділення нирками. Діяльність органів і систем, що забезпечують водно-сольовий гомеостаз, координується ЦНС. В процесі еволюції зростає точність і ефективність механізму регуляції. Кров (sanguis), циркулююча в кровоносній системі всіх хребетних і деяких безхребетних тварин - «рідка тканина внутрішнього середовища, являється тканиною, забезпечує життєдіяльність ін. тканин і клітин, а також виконання ними різних. функцій в цілісному організмі. Основні функції К.: дихальна - транспортує гази (О2 - від органів дихання до тканин і СО2 - від тканин до органів дихання); трофічна і екскреторна - переносить поживні речовини (глюкозу, амінокислоти, солі і т. п.) від органів травлення до тканин, а кінцеві продукти обміну (сечовина, креатин і ін.) - до органів виділення; регуляторна - бере участь в гуморальній регуляції (переносить гормони і ін. біологічно активні речовини), підтримує водно-сольовий обмін і кислотно-лужну рівновагу, грає важливу роль в підтримці постійної температури тіла; захисна - містить антитіла, антитоксини, лізіни, а також лейкоцити, здатні руйнувати і поглинати чужорідні агенти. Плазма містить проміжні і кінцеві продукти обміну речовин, солі, гормони, вітаміни, ферменти. Істотну частину крові складають білки - дихальні пігменти, білки строми еритроцитів і ін. формених елементів, а також білки плазми - альбуміни, глобуліни і фібріноген (плазма без фібріногену - сироватка крові). Вуглеводи представлені головним чином глюкозою. Складна суміш ліпідів крові включає нейтральні жири, вільні жирні кислоти і продукти їх розпаду, холестерин, стероїдні гормони і ін. У людини об'єм крові у нормі складає в середньому у чоловіків 5,2 л, у жінок 3,9 л, при цьому її частина, іноді до 50%, може знаходитися в т.з. депо крові (селезінка, печінка).
Серед незвичайних властивостей води важко обійти увагою ще одне – її виключно високе поверхневе натягнення 0,073 Н/м (при 20°С). Зі всіх рідин болем високе поверхневе натягнення має тільки ртуть. Воно виявляється в тому, що вода постійно прагне стягнути, скоротити свою поверхню, хоча вона завжди приймає форму ємкості, в якій знаходиться в даний момент. Вода лише здається безформною, розтікаючись по будь-якій поверхні. Сила поверхневого натягнення примушує молекули її зовнішнього шару зчіплюватися, створюючи пружну зовнішню плівку. Властивості плівки також визначаються замкнутими і розімкненими водневими зв'язками, асоціатами різної структури і різного ступеня впорядкованості. Завдяки плівці деякі предмети, будучи важчі за воду, не занурюються у воду (наприклад, обережно покладена на воду сталева голка).
Сольовий склад річкових і морських вод різний не тільки кількісно, але і якісно. На 89% морські солі складаються з хлоридів (переважно – натрію і кальцію), на 10%–з сульфатів (натрію, калія і магнію), на 1% – з карбонатів (натрію і кальцію), а також незначних кількостей інших солей. У прісних водах набір мінеральних домішок виглядає інакше. Більше всього тут карбонатів (натрію і кальцію) –до 80%. Сульфатів (натрію, кальцію і магнію)– біля 13%. 7% приходяться на хлориди (натрію і кальцію) і інші солі. З газів в прісних і морських водах найширше представлені кисень, азот, вуглекислий газ, сірководень. У чистих холодних стоках гірських річок зміст кисню може досягати 6 мг/л. У глибинних шарах Чорного моря висока концентрація сірководню – до 100 мг/л. Цей отруйний газ присутній і в нижніх шарах деяких озер. У прісних і морських водах в невеликих кількостях є і різноманітні органічні компоненти – розчинні з'єднання типу білків, цукрів, спиртів, вуглеводів. Це продукти життєдіяльності і розпаду тваринних і рослинних організмів, що населяють водоймища і їх береги, а також відходи промисловості і сільського господарства.
Капілярність води При вивченні цього явища встановили, що всі речовини, які легко змочуються водою (глина, пісок, скло, папір і ін.), неодмінно мають в своєму складі атоми кисню. Для пояснення природи змочування цей факт виявився ключовим: енергетично неврівноважені молекули поверхневого шару води дістають можливість утворювати додаткові водневі святи з «сторонніми» атомами кисню. Завдяки поверхневому натягненню і здібності до змочування, вода може підніматися у вузьких вертикальних каналах на висоту більшу ніж та, яка допускається силою тяжіння, тобто вода володіє властивістю капілярності. Капілярність грає важливу роль в багатьох природних процесах, що відбуваються на Землі. Завдяки цьому вода змочує товщу ґрунту, лежачу значно вище за дзеркало ґрунтових вод і доставляє корінню рослин розчини живильних речовин. Капілярністю обумовлено рух крові і тканинних рідин в живих організмах.
Епідеміологічне значення води.
Основу мікробної клітини складає вода - 80 - 90 % загальної маси. Вода є переносником мікроорганізмів як сапрофітних так і хвороботворних.
Escherichia coli серотип O157:H7 - основна причина розладів травлення. Інфекція викликана цією бактерією часто приводить до кривавого проносу, і іноді до ниркового недоліку. Люди можуть заразитися з E.coli O157:H7 багатообразними шляхами. Заразитися можна п'ючи заражену для стічних вод воду.
Холера - гостра інфекційна хвороба, викликана інфекцією кишечнику бактерійним вібріоном cholerae.
Люди стають зараженими Leptospira через контакт з водою, продовольством, або сечею, що містить лептоспір, від цих заражених тварин. Це, можливо, трапляється під час ковтання зараженого продовольства або води або через контакт шкіри, особливо з поверхнями, які відносяться до слизової оболонки, як наприклад очі або ніс, або з розбитою шкірою
Солі.
неорганічних речовин перебувають в організмі або в іонному стані, або у вигляді твердих сполук. Катіони – калію, кальцію, натрію, магнію, тощо. Аніони – соляної , сірчаної, фосфорної, вугільної, тощо.
В сучасному світі важливу роль відіграють заходи щодо зниження рівня забруднення довкілля деякими хімічними елементами, неорганічними і органічними сполуками.
Мільярди років тому в холодній газопиловій хмарі, що з часом згустилася, ущільнилася і стала Землею, вже містилася вода. Швидше за все, вона була у вигляді крижаного пилу. Це підтверджують дослідження Всесвіту. Уставлено, що початкові елементи для утворення води — водень і кисень в нашій Галактиці належать до найпоширеніших речовин космосу.
Фізіологічне значення води
Добова потреба в воді – 1,5 і більше літрів на людину. З віком кількість води знижується. При порушенні водного балансу відбувається ряд порушень.
Гігієнічне значення води.
Добова потреба води залежить від регіону може досягати до 1000 літрів на людину. За відсутності центрального водопостачання 60 л.
Класифікація забруднення води:
1. Хвороботворними організмами.
2. Хімічне забруднення води
А. Неорганічними;
Б. Органічними;
В. Токсичними;
Г. Поверхнево-активними сполуками;
Епідеміологічне значення води. Близько напівмільярда людей хворіє на захворювання, які передаються через воду, 3 мільйони гине.
1. Бактерійні антропонози (дизентерія, холера)
2. Вірусні (гепатит, поліомієліт)
3. Зоонозні інфекції (лептоспіроз).
4. Паразитарні захворювання - захворювання лямбліоз), гельмінтози (геогельмінти)
5. Ендемічні захворювання. Пов'язані з мінеральним складом води.
Умови для розповсюдження хвороб: збудник повинен потрапити у воду, патогенні мікроорганізми повинні зберігати активність у воді, збудник повинен потрапити в організм.
Епідеміологічна характеристика спалахів захворювань.
1. Масовість (дифузна) При залповому забрудненні мікроорганізм може потрапити у водопровідну мережу і викликати захворювання.
2. Сезонність (рання весна)
3. За етіологічністю.
4. За клінікою: поліморфізм (різна по ступеню тяжкості клінічна картина)
5. Зниження ступеня тяжкості захворювань в динаміці.
6. Різкий підйом і повільний спад.
При харчовому: спалахи хвороби, різкий підйом і спад, приблизно однакові клінічні прояви.
Хімічний склад води.
1. Хімічні речовини присутні в будь-якому випадку.
2. Хімічні речовини, що потрапляють у воду в результаті дії людини.
Мінеральний склад води. У воді загальна мінералізація – хлориди сульфати. Впливають на органолептичні властивості.
Загальна мінералізація - солі хлору і сірки. Не вище 1 г на літр. Для питної води не більше 1г на літр. Якщо більше грама - мінеральна вода. Питна вода повинна бути без смаку. Мінеральна вода - з присмаком. Нормальна питна вода - 200-400 мг на літр. Вода з показниками вище - є слабкомінералізованою.
Жорсткість води. Постійна і усунена жорсткість. Усунена - при кип'яченні випадають в осад.
При зміні жорсткості води можуть спостерігатися диспепсичні розлади. До 7 міліграм на літр.
Азотисті сполуки. Визначаються в будь-якій воді. Утворюються при окисненні органічних речовин у воді. При кип'ятінні знищуються сапрофітні бактерії, що з часом приводить до погіршення органолептичних властивостей води.
Коло обіг нітрогену в воді:
Аміак—нітрити—нітрати.
По концентрації цих сполук можна говорити про органічне забрудення води.
Метгемоглобінемію викликають нітрити.
Ендемічні захворювання.
Флюороз. Проявляється зміною суглобів. Остеопороз, тугорухливість суглобів.
Ендемічний зоб. Нестача в воді йоду, або наявність великої концентрації сполук, які його зв’язують
Хімічні речовини, що ПОТРАПЛЯЮТЬ У ВОДУ, ЧАСТО МАЮТЬ АНТРОПОГЕННУ ДІЮ.
В РОЗЧИНЕНОМУ СТАНІ БІЛЬШЕ 3000 ХІМІЧНИХ СПОЛУК у водоймищах.
ГДК - гранично допустима концентрації.
1. Вивчення вплив речовини на органолептичні властивості води.
2. Вивчення токсичних властивостей речовини.
3. Вплив речовини на процеси самоочищення водоймищ.
Визначається лімітуючий показник, на підставі якого встановлюється ГДК.
Якість води – вивчення:
1 етап - органолептичні властивості.
2 етап - почало 19 століття. У Брюсселі документ, що НОРМУЄ хімічний склад води
3 етап - мікробіологічні показники.
4 етап - всі разом з середини минулого століття.
Вимоги до питної води.
1. Повинна відповідати безпеці, нешкідлива і сприятлива.
2. Якість води повинне відповідати нормі не тільки на водопровідній станції, але і в місцях використання.
3. Безпека питної води визначається по нормативу, що характеризує мікробну, вірусну і паразитарну дію.
4. Нешкідливість визначається по 3 групам показників
А. Узагальнені показники хімічних речовин, які містяться в природних умовах.
Б. Ті що утворюються у воді при очищенні або знезараженні.
В. Токсичні хімічні речовини.
5. Мікробіологічні показники.
Органічне забруднення води
Визначається по азотистих з'єднаннях.
Окислюваність води - та кількість кисню, яка необхідна для окислення органіки.
Біохімічна потреба кисню - та кількість кисню, яка необхідна для біохімічного окислення води.
Мікробіологічні показники.
Паразитарне забруднення
Водневий показник Нормативи 6-9 рН
Гігієнічні вимоги щодо якості питної води та її санітарна оцінка на Україні. В Україні ці вимоги регламентовані санітарним законодавством - документом ДСАНПіН (Державні санітарні правила і норми «Вода питна». Гігієнічні вимоги до якості води централізованого господарсько-питного водопостачання № 383 від 23. 12. 1996 р.)
Мікробіологічну чистоту води визначають за такими параметрами:
Мікробне число води це – кількість мікробів в 1 мл води.
Визначення колі-індексу.
Визначення колі титру.
Визначення вмісту хлору у воді;
Визначення залишкового хлору у питній воді.
ПДК за мікроорганізмами води для пиття.
Колі-титр води – мінімальна кількість води, в якій виявляють бактерії групи кишкової палички – норми визначення не менше 300
Колі-індекс води– це кількість кишкової палички в 1 л води – норми визначення не більше 3.
Жодної цисти лямблій в 50 літрах води.
Централізоване водопостачання.
Гігієнічна характеристика джерел водопостачання.
Вимоги: доступність вододжерела, достатня водоємність джерела. Повинна бути в 1000 разів більше, НІЖ необхідно для населеного пункту, інтенсивність забруднення повинна піддаватися усуненню.
Джерела води: підземні, поверхневі.
Розташування джерел води.
Проточні і непроточні. Вода відкритих вододжерел коливається за складом залежно від пори року. Найбільш стабільними в цьому показники є оліготрофні озера. На глибині 10м забруднення і склад постійні.
Підземні води найбільш якісні. Діляться на ґрунтові і міжпластові. Глибина залягання - 2-4 метри.
Найбільш хороша - міжпластова.
Свердловини бувають напірні або артезіанські і безнапірні.
Якість води зі свердловин оптимальна. Хімічний склад залежить від геологічного складу ґрунту.
Методи очищення:
Барабанні мікро фільтри - від грубої суспензії. Розмір часток 0.1мм. Близько 40% частинок затримуються. Майже 100% розчинених сполук не затримуються.
Коагуляція Процес укрупнення колоїдних домішок за рахунок їх взаємного злипання. Солі алюмінію, заліза. До 80% хімічних речовин адсорбуються. Додають флоккулянти - сполуки, прискорюючі коагуляцію.
Відстоювання води.
У відстійниках флокційні методи є додатковими при відстоюванні. Особливості - для видалення поверхнево-активних речовин.
Фільтрація води - Піщані фільтри. 1-1.5 м. Повільна і швидка фільтрація. Найбільш небезпечна з погляду хімічної сполуки. Насипні, іонообмінні фільтри, полупроникні мембрани. Адсорбційні фільтри. Активоване вугілля, де структура фільтру нагадує сир.
Знезараження води. Може бути хімічним і фізичним.
При використанні фізичних методів неможливо швидко визначити якість води. 90% води в світі хлорується. Використовується газоподібний хлор частіше за все при централізованому водопостачанні в крупних містах. Активну дію забеспечує або хлор, або хлоорноватиста кислота.
Гідробіологія, це наука про екологію води – наука, що вивчає взаємини людини, тварин. рослин. інших живих організмів з водневим навколишнім середовищем. Людина безпосередньо залежить від екологічної рівноваги, яка зберігає стабільність умов навколишнього середовища, без якого людина не мала б шансів вижити. А як відомо – основою життя на Землі є вода. У природі існує відносна стійкість видового складу живих організмів, їх чисельності, продуктивності, розподілу в просторі, а також сезонних змін, біотичний. колообіг речовин в будь-яких природних співтовариствах. Існує колообіг і води. Людина випиває і з’їдає за своє життя більше 50 тон води, білків біля 2,5 тон, жирів біля 2,0 тон, вуглеводів – 10 тон, солі – 30 кг. Накопичення майже незначної кількості шкідливих речовин в продуктах харчування може протягом часу призводити до значних змін з боку органів і систем і в решті решт негативно впливати на стан здоров’я людини .









